▼Kesimpta® (ofatumumab) [1]
Kesimpta® (ofatumumab) er er et fullstendig humant monoklonalt antistoff. Dette er den første og eneste selvadministrerte, målrettede B-celleterapibehandlingen for voksne pasienter med relapserende multippel sklerose (RMS).1

Illustrasjon: Kesimpta® (ofatumumab) kommer med en ferdigfylt penn. Der hver ferdigfylte penn inneholder 20 mg ofatumumab i en 0,4 ml oppløsning.
Nasjonalt kvalitets- og kompetansenettverk for multippel sklerose (MS) har i sitt nyhetsbrev kommet med anbefalinger for medisinske indikasjoner for bruk av Kesimpta der andre rimeligere anti-CD20 antostoff er vurdert uegnet.2
Disse er:
- Ved serumsyke etter rituksimab infusjon (feber, artralgi og utslett 1-2 uker etter infusjon) og samtidig manglende tap av CD19+ B-celler under behandling med rituksimab.
- Ved alvorlige, potensielt livstruende infusjonsreaksjoner under rituksimab behandling (kan forventes hos mindre enn 1 % av pasienter behandlet med rituksimab).
- Ved behandlingssvikt under rituksimab behandling, med nye MS-attakk og nye MRI-lesjoner med eller uten kontrastlading, oppstått etter en oppstartsperiode på 3-6 måneder. Dette kan særlig vurderes hos pasienter som i tillegg har manglende/lavt fall av CD19-positive celler 1-2 måneder etter behandling.
- Pasienter med lavt IgG (anslagsvis <= 7 g/L ) før oppstart med aCD20, og der man likevel anser aCD20 som beste behandling.
- Pasienter som under behandling med rituksimab har betydelig og vedvarende fall i IgG (anslagsvis 1-2 g/l per år over en periode på 2-3 år), og der aCD20 likevel anses som beste behandling. Som hovedregel anbefales forlenget intervall mellom rituksimabinfusjonene før bytte til ofatumumab. Grensen for hva som er betydelig fall i IgG vil avhenge av IgG-nivået før oppstart av rituksimab, og om det også er andre tegn til svekket infeksjonsforsvar som lymfopeni, nøytropeni eller infeksjonstendens.
Sikkerhet
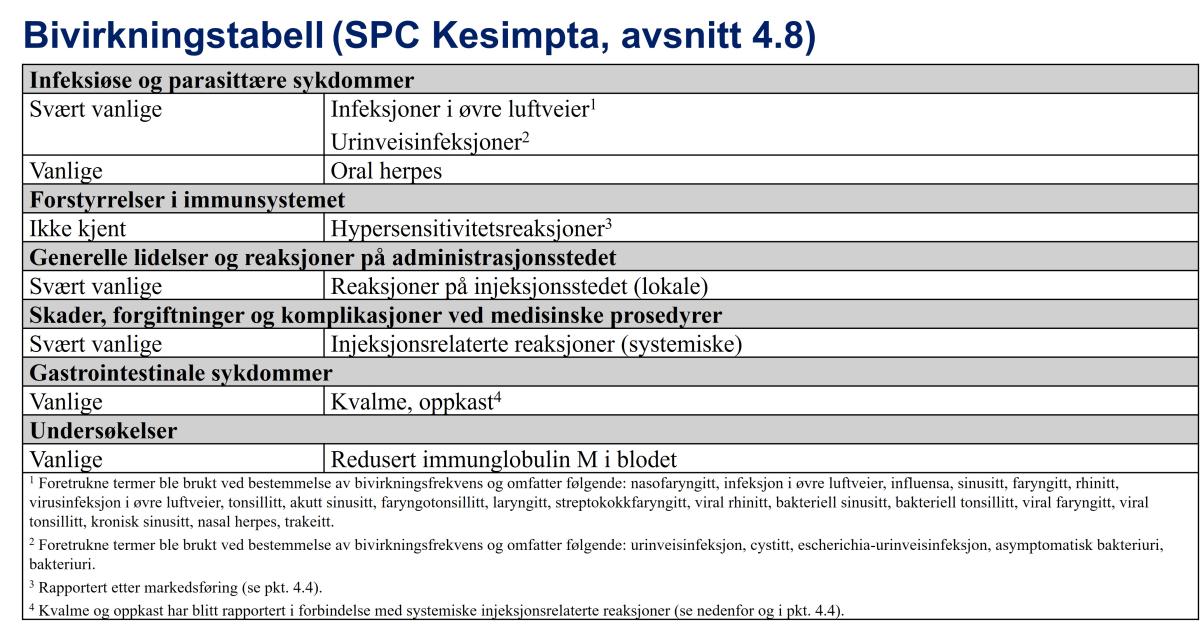
Bivirkninger som har vært rapportert i forbindelse med bruk av ofatumumab i pivotale kliniske studier ved RMS og etter markedsføring, er oppgitt i tabell 1 i henhold til MedDRAs organklassesystem. Innen hver organklasse er bivirkninger rangert etter frekvens, med de hyppigst forekommende reaksjonene først. Innen hver frekvensgruppering er bivirkninger presentert etter synkende alvorlighetsgrad. I tillegg er de tilsvarende frekvenskategoriene for hver bivirkning basert på følgende inndeling: svært vanlige (≥ 1/10), vanlige (≥ 1/100 til < 1/10), mindre vanlige (≥ 1/1 000 til < 1/100), sjeldne (≥ 1/10 000 til < 1/1 000), svært sjeldne (< 1/10 000), ikke kjent (kan ikke anslås ut ifra tilgjengelige data).
Viktig sikkerhetsinformasjon:
- Pasientene bør informeres om at systemiske injeksjonsrelaterte reaksjoner kan forekomme, vanligvis i løpet av 24 timer og hovedsakelig etter første injeksjon 1
- Det anbefales å undersøke pasientens immunstatus før behandling igangsettes. Kvinner som kan bli gravide, må bruke effektiv antikonsepsjon1
- Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Alvorlig nedsatt immunforsvar. Alvorlig aktiv infeksjon inntil bedring. Kjent aktiv malignitet1
- Hyppigste bivirkninger: Infeksjoner i øvre luftveier, systemiske injeksjonsrelaterte reaksjoner, reaksjoner på injeksjonsstedet og urinveisinfeksjoner1
Reseptgruppe, refusjon & pris: Reseptgruppe C. H-resept. Kesimpta 20 mg, 1 stk. (ferdigfylt penn). Listepris (AUP) Kr 22 101,00 per 05.09.2024. Endelig pris er rabattert. Godkjent av Beslutningsforum (ID2020_066:): Til behandling av voksne med relapserende former for multippel sklerose (RMS) med aktiv sykdom definert ved kliniske eller bildediagnostiske funn når annet, rimeligere anti-CD20 antistoff er vurdert uegnet. For mer informasjon, se felleskatalogen.no